Dénes Ádám (HUN-REN Kísérleti Orvostudományi Kutatóintézet) és Miao Jing (Brain Institute CAS, Sanghaj) kutatócsoportjainak együttműködése feltárta, miként szabályozza az agy az akut sérülésekre adott válaszreakciók erősségét és kiterjedését.
Dénes Ádám kutatócsoportja fedezte fel, hogy a mikroglia ATP-érzékelés révén alakít ki funkcionális kapcsolatokat az idegsejtek sejttestjével, és agyi fertőzések esetén is a lokális ATP-felszabadulás alapján azonosítja az érintett idegsejteket. Az agyban az ATP tehát nem csak a sejtek energiaforrásaként szolgál, de az egyik legfontosabb sérülést jelző molekula is egyben. Az idegrendszeri kutatások egyik legnevesebb nemzetközi folyóiratában, a Neuronban most megjelent cikk azt a kérdéskört vizsgálja, hogyan kontrollálja az agy az akut sérülésekre adott válaszreakció mértékét térben és időben. Ezekben a folyamatokban az ATP szintén központi szereplő lehet.
A mikroglia sérülésérzékelő képességének vizsgálatára Dénes Ádám és Miao Jing 2020-ban nyertek egy Kínai-Magyar TéT pályázatot.
A Miao Jing laboratóriumában létrehozott, és az együttműködés eredményeként továbbfejlesztett G–protein kapcsolt receptor (GPCR) alapú, új generációs bioszenzorok az agyi ATP valós idejű képalkotó méréseihez lettek optimalizálva. A GPCR alapú szenzorok korábban elképzelhetetlen, nanomolos érzékenységgel teszik láthatóvá az agyi parenchymában és az erek környezetében a különböző purin mediátorok felszabadulását, így alkalmasak a neuroimmun interakciók és idegrendszeri kórfolyamatok vizsgálatára.
Miao kutatócsoportjának 2024-es, a Nature Neuroscience-ben megjelent munkájából kiderült, hogy az asztrociták fokális sérülés esetén ritmikus ATP felhőket bocsátanak ki, amelyek a sejten belüli (intracelluláris) ATP koncentráció százezredével is képesek a mikroglia nyúlványok toborzására. Nem volt világos azonban, hogy a mikrogliális válasz milyen módon hat vissza az asztrocita sejtek ATP termelésére, és ennek milyen hatása van az inzultust követő agyi sérülés vagy a neuronhálózati zavarok kialakulására. A kutatók feltárták, hogy a mikroglia sejtekből felszabaduló proinflammatorikus citokin, az interleukin-1 beta (IL-1b) negatív visszacsatolással szabályozza az asztrocita ATP-termelést és ezáltal korlátozza az agyi sérülés térbeli és időbeli kiterjedését. Ez azért is különösen figyelemre méltó, mert az IL-1b globális gátlása a legtöbb agyi sérülésmodellben (agyi trauma, stroke) klinikai adatok szerint is javítja a kimenetelt.
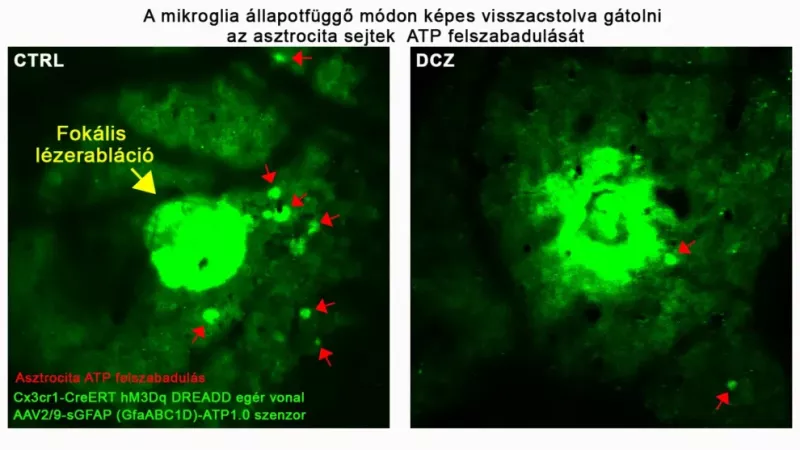
Kiderült az is, hogy a sérülés mértéke meghatározó: agyi mikrosérülések esetén a mikrogliális IL-1b termelés vélhetően egy evolúciósan konzervált, hasznos folyamat a sérülés kiterjedésének gátlására, míg nagyobb méretű agyi sérülés vagy gyulladás során ez az egyensúly felborulhat, gátolva vagy akár megfordítva a negatív visszacsatolás hatékonyságát.
A koncepció közös kidolgozása alapján a kísérletes munka oroszlánrésze a kínai laborban készült, a Dénes-laborban pedig kulcsfontosságú mikroglia-manipulációs és -validációs kísérleteket végeztek. Környei Zsuzsa több modellben is megmutatta, hogy a mikroglia puszta jelenléte, illetve az IL-1b hozzáadása is korlátozza az asztrocitához köthető ATP-események kialakulását, Schwarcz Anett pedig in vivo két-foton mikroszkópos mérésekkel igazolta a mikroglia-asztrocita interakciók ATP-függő dinamikáját a laborban kidolgozott MicroDREADD egérvonal felhasználásával.
Valós idejű képalkotó mérések nélkül nem megoldható az agyi sérülés- és immunfolyamatok komplexitásának megértése, és ebben – különösen az egyszerű, gyorsan metabolizálódó molekulák, mint az ATP esetén – az új generációs, GPCR alapú bioszenzorok már eddig is nagy horderejű tudományos felfedezéseket tettek lehetővé. Alkalmazásuknak egy újabb, izgalmas és sok meglepetést tartogató területe az agyi neuroimmun folyamatok vizsgálata.
Forrás: hellosajto.hu







